Classificatie
Complerais een geneesmiddel met een vaste tablet met één tablet dat wordt gebruikt voor de behandeling van HIV, dat bestaat uit drie verschillende antiretrovirale middelen:
- rilpivirine, a niet-nucleoside reverse transcriptase-remmer (NNRTI)
- emtricitabine, een nucleotide reverse transcriptase-remmer (NtRTI)
- tenofovirdisoproxilfumaraat (TDF), een andere NtRTI
Complera werd op 10 augustus 2011 door de Amerikaanse Food and Drug Administration (FDA) goedgekeurd voor gebruik bij zowel volwassenen als kinderen ouder dan 12 jaar die nog nooit HIV-therapie hebben gehad, die een virale lading hebben van 100.000 cellen / m of minder, en wegen 77 pond (35 kg) of meer.
Complera kan ook worden gebruikt om een huidige therapie te vervangen als de patiënt een niet-waarneembare virale last heeft gehad (
Formulering
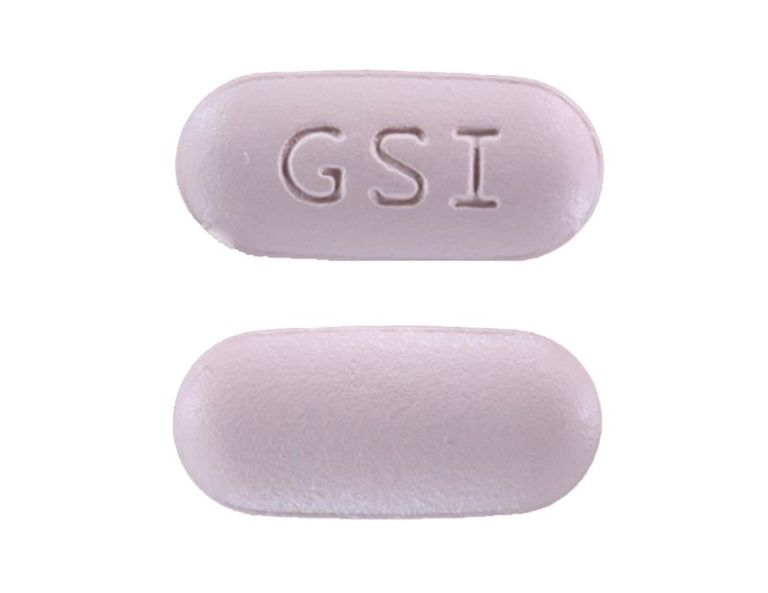
Complera is een roze, capsulevormige filmomhulde tablet, bestaande uit 25 mg rilpivirine, 200 mg emtricitabine en 300 mg TDF Het heeft de inscriptie "GSI" aan de ene kant en is duidelijk aan de andere kant.
Dosering
Eén tablet per dag ingenomen met voedsel Complera mag niet worden ingenomen met andere antiretrovirale geneesmiddelen die worden gebruikt voor de behandeling van HIV.
Bijwerkingen
Een getal van bijwerkingen van geneesmiddelen zijn geconstateerd bij patiënten op de klinische proef met Complera, waarvan de meest voorkomende waren:
- Misselijkheid
- Hoofdpijn
- Slapeloosheid
- Depressie
Bijwerkingen waren in het algemeen voorbijgaand, met weinig patiënten die stopten als gevolg van intolerantie van de behandeling.
Contra-indicaties
Complera dient niet te worden ingenomen met de volgende geneesmiddelen of supplementen: Anti-convulsieve medicatie: Tegretol, Trilepta, fenobarbital, fenytoïne Anti-tuberculose medicatie: Mycobutin, Rifater, Rifamate, Rimactane, Rifadin, Priftin
- Protonpompremmers (PPI’s): Nexium, Kapidex, Dexilant, Prevacid, Losec, Prilosec, Protonix, Aciphex of andere PPI
- Steroid medicatie: dexamethason (hoewel het in een enkele dosis kan worden toegediend als medisch geïndiceerd)
- Sint-janskruid
- Informeer uw arts altijd over elk geneesmiddel of supplement, al dan niet voorgeschreven, dat u mag nemen voordat u begint met een antiretrovirale therapie.
- Andere overwegingen
Complera wordt niet aanbevolen voor patiënten met nierinsufficiëntie (gedefinieerd als hebbende een geschatte creatinineklaring van minder dan 30 ml per minuut). Vertel uw arts als u bent of wordt behandeld voor een nieraandoening door een andere arts.
Complera wordt niet aanbevolen voor patiënten met een leverfunctiestoornis of voor patiënten met een chronische hepatitis-B-infectie (HBV), aangezien dit de leverproblemen ernstig kan verergeren. Het wordt geadviseerd om personen met HIV op HBV te screenen voordat ze Complera voorschrijven. Vertel uw arts als u leverproblemen en / of een voorgeschiedenis van hepatitis heeft.
De rilpivirine-component van Complera kan een overgevoeligheidsreactie veroorzaken bij een klein aantal patiënten, vaak in de vorm van huiduitslag, oogontsteking ("roze oog"), zwelling van het gezicht, koorts of andere allergische reacties. Over het algemeen zijn overgevoeligheidsreacties 1-6 weken na het begin van de therapie aanwezig. Breng uw arts onmiddellijk op de hoogte van dergelijke symptomen. In ernstige gevallen zal de behandeling waarschijnlijk moeten worden gestaakt.
Behandelingsupdate
Een nieuwere formulering van Complera werd op 1 maart 2016 door de FDA goedgekeurd, op de markt gebracht onder de naam Odefsey. Deze nieuwere formulering vervangt de TDF-component door een geneesmiddel genaamd tenofoviralafenamide (TAF), waarvan de laatste wordt geclassificeerd als een pro-drug.

